第一章 单元测试
与仪器分析相比,化学分析的优势包括( )。
选项:
A:准确度高
B:灵敏度高
C:分析成本低
D:选择性好
答案: 【准确度高;
分析成本低】
2、单选题:
溶液中,离子的活度数值小于其浓度数值的原因是( )。
选项:
A:数值测量存在误差
B:溶液中的中性分子过多
C:溶液中的离子过少
D:离子周围聚集带相反电荷的离子,形成了离子氛
答案: 【离子周围聚集带相反电荷的离子,形成了离子氛】
3、判断题:
滴定分析中,低浓度NaOH溶液是标准溶液。所以,NaOH是基准物质。( )
选项:
A:对
B:错
答案: 【错】
4、单选题:
滴定分析的最大固有相对误差约为( )。
选项:
A:0.1%
B:0.2%
C:0
D:无法确定
答案: 【0.1%】
5、单选题:
关于化学平衡等量关系,错误的叙述是( )。
选项:
A:一个平衡体系可以有多个物料平衡式
B:电荷平衡式不独立于物料平衡式
C:一个平衡体系只有一个电荷平衡式
D:质子平衡式是独立等量关系
答案: 【质子平衡式是独立等量关系】
第二章 单元测试
1、单选题:
关于系统误差,错误的叙述是( )。
选项:
A:影响有正有负
B:具有再现性
C:源自确定性因素
D:可以减小甚至消除
答案: 【影响有正有负】
2、单选题:
关于有效数字,错误的叙述是( )。
选项:
A:零不计入有效数字
B:有效数字反映测量精度
C:pH = 10.82表明2位有效数字
D:有效数字应当采用科学计数法
答案: 【零不计入有效数字】
3、单选题:
关于系统误差传递,错误的叙述是( )。
选项:
A:只涉及加减的计算式,传递的是绝对误差
B:误差传递结果与直接测量值的大小无关
C:计算基于全微分
D:只涉及乘除的计算式,传递的是相对误差
答案: 【误差传递结果与直接测量值的大小无关】
4、判断题:
数理统计应用的关键:随机变量的分布、通过该分布获得概率和相应临界值。( )
选项:
A:错
B:对
答案: 【对】
5、单选题:
正态分布的PDF曲线越窄,说明( )。
选项:
A:总体方差越小
B:总体均值越大
C:总体方差越大
D:总体均值越小
答案: 【总体方差越小】
6、多选题:
欲研究样本方差,可以使用的分布有( )。
选项:
A:F分布
B:正态分布
C:t分布
D:卡方分布
答案: 【F分布;
卡方分布】
7、单选题:
能够得出统计显著结论的是( )。
选项:
A:检验统计量的取值大于临界值
B:检验统计量的取值小于临界值
C:P-值大于显著性水平
D:P-值小于显著性水平
答案: 【P-值小于显著性水平】
第三章 单元测试
1、单选题:
关于分布分数,错误的叙述是( )。
选项:
A:分布分数与酸碱组分的浓度有关
B:分布分数是关于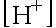 或者
或者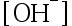 的代数式
的代数式
C:分布分数能够显著简化推导
D:某酸(或者某碱)的所有组分的分布分数之和等于1
答案: 【分布分数与酸碱组分的浓度有关】
2、多选题:
酸碱平衡的定量解析中,电荷平衡式CBE的优点包括( )。
选项:
A:CBE具有惟一性
B:CBE容易列出
C:CBE是独立于物料平衡式的一个等式
D:CBE不易出错
答案: 【CBE具有惟一性;
CBE容易列出;
CBE不易出错】
3、判断题:
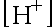 的去公式化计算,可以概括为从CBE出发,结合分布分数推导出关于
的去公式化计算,可以概括为从CBE出发,结合分布分数推导出关于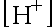 或者
或者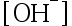 的方程,最后求解。( )
的方程,最后求解。( )
选项:
A:对
B:错
答案: 【对】
4、判断题:
Na2CO3和NaHCO3混合溶液,二者的分析浓度均为0.010 mol×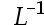 。该溶液的
。该溶液的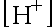 代数方程为
代数方程为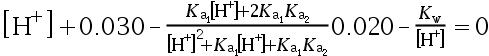 。( )
。( )
选项:
A:错
B:对
答案: 【对】
5、单选题:
关于缓冲溶液,错误的叙述是( )。
选项:
A:pH = pKa
B:通常由共轭酸碱对组成
C:(分别用于抵抗外加酸和碱的)缓冲组分的量一般设为相同
D:缓冲组分的浓度较高
答案: 【pH = pKa】
6、单选题:
一元强碱滴定一元强酸时,( )。
选项:
A:滴定突跃的大小与组分浓度无关
B:滴定剂浓度越大,滴定突跃越大
C:被测物浓度越大,滴定突跃越大
D:滴定突跃的大小与指示剂有关
答案: 【被测物浓度越大,滴定突跃越大】
7、单选题:
以0.010 mol×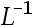 HCl溶液滴定同浓度的氨水,已知Kb = 1.8×
HCl溶液滴定同浓度的氨水,已知Kb = 1.8×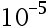 。以甲基橙(pHep = 8.5)为指示剂的终点误差是( )。
。以甲基橙(pHep = 8.5)为指示剂的终点误差是( )。
选项:
A:1.0%
B:0.2%
C:2.0%
D:0.1%
答案: 【0.2%】
8、多选题:
关于酸碱准确滴定判别,正确的叙述是( )。
选项:
A:一元弱酸准确滴定的判别式为Kacsp ≥ 10-8
B:判断±0.2 pH偏移导致的误差是否超出0.1%
C:判断滴定突跃是否大于0.4 pH单位
D:用于判断酸碱滴定方案是否可行
答案: 【一元弱酸准确滴定的判别式为Kacsp ≥ 10-8;
判断±0.2 pH偏移导致的误差是否超出0.1%;
判断滴定突跃是否大于0.4 pH单位;
用于判断酸碱滴定方案是否可行】
第四章 单元测试
1、单选题:
以下叙述错误的是( )。
选项:
A:EDTA滴定需要缓冲溶液来控制酸度
B:EDTA滴定是配位滴定的主要内容
C:EDTA与大多数金属离子生成1:1螯合物
D:EDTA螯合物通常是无色的
答案: 【EDTA螯合物通常是无色的】
2、单选题:
表观浓度与平衡浓度的关系是( )。
选项:
A:表观浓度小于或者等于平衡浓度
B:表观浓度大于平衡浓度
C:表观浓度大于或者等于平衡浓度
D:表观浓度小于平衡浓度
答案: 【表观浓度大于或者等于平衡浓度】
3、多选题:
EDTA配位滴定中,EDTA的副反应系数( )。
选项:
A:与氢离子的平衡浓度有关
B:与干扰金属离子的平衡浓度有关
C:与干扰配体的平衡浓度有关
D:与干扰金属离子的分析浓度有关
答案: 【与氢离子的平衡浓度有关;
与干扰金属离子的平衡浓度有关】
4、判断题:
EDTA配位滴定中,至少存在一个副反应。( )
选项:
A:错
B:对
答案: 【对】
5、单选题:
关于EDTA配位滴定曲线,错误的叙述是( )。
选项:
A:纵坐标是金属离子M的表观浓度的负对数
B:通过反函数可以方便绘制高精度滴定曲线
C:纵坐标也可以是金属离子M的平衡浓度的负对数
D:曲线与酸效应无关
答案: 【曲线与酸效应无关】
6、单选题:
如果金属离子M与指示剂的稳定常数大于M与EDTA的稳定常数,那么( )。
选项:
A:出现指示剂封闭现象,没有终点
B:会使终点提前
C:对滴定终点判断没有影响
D:会使终点滞后
答案: 【出现指示剂封闭现象,没有终点】
7、单选题:
用0.020 mol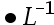 EDTA溶液滴定同浓度的Mg2+溶液,控制pH = 10.00,以EBT为指示剂。已知KMgY = 5.01
EDTA溶液滴定同浓度的Mg2+溶液,控制pH = 10.00,以EBT为指示剂。已知KMgY = 5.01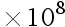 ,
,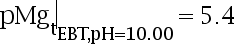 ,
,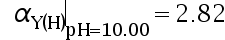 ,那么终点误差为( )。
,那么终点误差为( )。
选项:
A:-0.10%
B:-0.20%
C:0.10%
D:0.20%
答案: 【0.10%】
8、多选题:
关于配位准确滴定判别,正确的叙述包括( )。
选项:
A:存在简单易用的判别式
B:有些判别式通过近似手段得到
C:酸碱准确滴定判别中的“终点误差法”和“滴定突跃法”依然有效
D:判别式从林邦公式导出
答案: 【存在简单易用的判别式;
有些判别式通过近似手段得到;
酸碱准确滴定判别中的“终点误差法”和“滴定突跃法”依然有效;
判别式从林邦公式导出】
第五章 单元测试
1、单选题:
如果 ,那么( )。
,那么( )。
选项:
A:没有反应发生
B:Red1还原Ox2
C:无法判断反应方向
D:Ox1氧化Red2
答案: 【Red1还原Ox2】
2、单选题:
关于条件电势,错误的叙述是( )。
选项:
A:使用条件电势的能斯特方程只包含氧化态和还原态的平衡浓度
B:指定介质后,条件电势为定值
C:条件电势替换能斯特方程中的标准电势,以提高准确性
D:条件电势从标准电势计算得到
答案: 【条件电势从标准电势计算得到】
3、单选题:
通过能斯特方程计算时,数值精度不够会导致误差,相对误差更大的是( )。
选项:
A:无法判断
B:浓度计算值
C:电势计算值和浓度计算值的相对误差相等
D:电势计算值
答案: 【浓度计算值】
4、单选题:
电对Ox1/Red1和Ox2/Red2的电子转移数均为1,且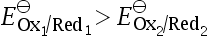 。欲使反应完成程度大于99.9%,那么
。欲使反应完成程度大于99.9%,那么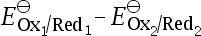 应大于( )。
应大于( )。
选项:
A:0.40 V
B:0.27 V
C:0.35 V
D:0.18 V
答案: 【0.35 V】
5、单选题:
化学计量点电势 ,该式的适用条件是( )。
,该式的适用条件是( )。
选项:
A:普适公式
B:两电对必须是可逆电对
C:反应物之一是对称电对即可
D:两电对必须是对称电对
答案: 【两电对必须是对称电对】
6、判断题:
如果滴定剂与被测物均为对称电对,那么滴定突跃与组分浓度无关。( )
选项:
A:错
B:对
答案: 【对】
7、单选题:
盐酸介质中,以0.10 mol∙L-1 Ce4+溶液滴定同浓度的Fe2+溶液,Eep = 0.84 V。已知Ce4+/Ce3+和Fe3+/Fe2+的条件电势分别为1.28 V和0.68 V,那么终点误差为( )。
选项:
A:1.9%
B:0.19%
C:-1.9%
D:-0.19%
答案: 【-0.19%】
第六章 单元测试
1、单选题:
下列沉淀反应,不属于银量法的是( )。
选项:
A: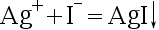
B: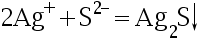
C: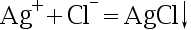
D: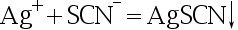
答案: 【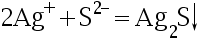
】
2、单选题:
沉淀溶解度的含义是( )。
选项:
A:1 L溶液中沉淀分子从固相到液相的转移量
B:溶液中构晶阳离子的浓度
C:溶液中构晶阳离子和构晶阴离子的浓度之和
D:溶液中构晶阴离子的浓度
答案: 【1 L溶液中沉淀分子从固相到液相的转移量】
3、多选题:
能够提高沉淀溶解度的因素有( )。
选项:
A:盐效应
B:配位效应
C:酸效应
D:同离子效应
答案: 【盐效应;
配位效应;
酸效应】
4、单选题:
均相沉淀法能够制备出颗粒大、杂质少的晶形沉淀,主要是因为( )。
选项:
A:增强了均相成核作用
B:快速沉淀
C:陈化作用
D:有效克服沉淀剂局部过浓问题
答案: 【有效克服沉淀剂局部过浓问题】
5、单选题:
将CaC2O4沉淀置于0.010 mol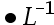 盐酸中,沉淀溶解时酸效应会( )。
盐酸中,沉淀溶解时酸效应会( )。
选项:
A:逐渐增强
B:不变
C:逐渐减弱
D:无法确定
答案: 【逐渐减弱】
6、单选题:
将MgNH4PO4置于蒸馏水,溶解平衡后[H+]=2.0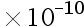 mol
mol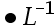 ,[Mg2+]=5.6
,[Mg2+]=5.6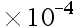 mol
mol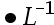 。已知NH3:Kb = 1.8
。已知NH3:Kb = 1.8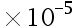 ;H3PO4:K1 = 7.6
;H3PO4:K1 = 7.6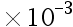 ,K2 = 6.3
,K2 = 6.3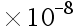 ,K3 = 4.4
,K3 = 4.4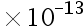 ,那么MgNH4PO4的溶度积常数等于( )。
,那么MgNH4PO4的溶度积常数等于( )。
选项:
A:1.8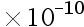
B:1.0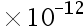
C:1.0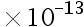
D:2.0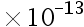
答案: 【1.0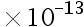
】
7、单选题:
将CaC2O4置于pH = 3.00的盐酸中,假设溶液原有H+浓度不受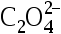 水解的影响,保持不变。已知CaC2O4:Ksp = 2.3
水解的影响,保持不变。已知CaC2O4:Ksp = 2.3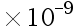 ;H2C2O4:K1 = 5.9
;H2C2O4:K1 = 5.9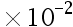 ,K2 = 6.4
,K2 = 6.4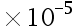 ,那么溶解度等于( )。
,那么溶解度等于( )。
选项:
A:1.8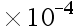 mol
mol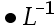
B:2.0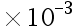 mol
mol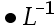
C:1.0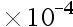 mol
mol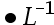
D:2.0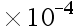 mol
mol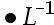
答案: 【2.0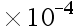 mol
mol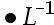
】









评论0